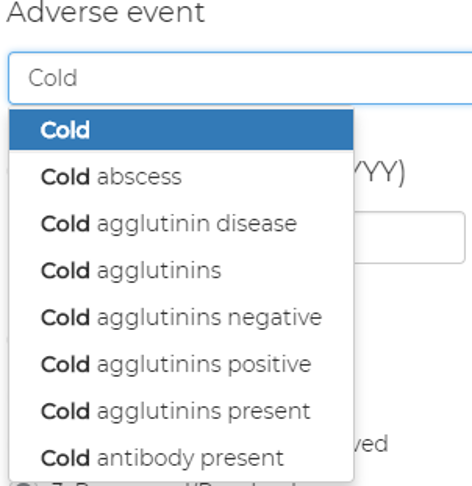
Uwaga!
- Wpisy otwarte (np. diagnoza, zdarzenia niepożądane, powody zakończenia udziału w badaniu, komentarze Badacza) są niezwykle trudne do analizy.
Rekomendacje:
- O ile to możliwe należy korzystać z terminologii kontrolowanej (słowników) - MedDRA, WHO Drug Dictionary.
- Źródłem informacji na temat dostępnych kontrolowanych terminologii w standardach CDASH/SDTM jest strona https://www.cancer.gov/research/resources/terminology/cdisc#2
-
Przykłady pól, dla których istnieje kontrolowana terminologia:
- Częstość przyjmowania leku;
- Droga podania leku;
- Powody zakończenia uczestnictwa w badaniu.